
高活性・高生産株のスクリーニング実験系を、速く・再現よく構築しませんか?
微生物・酵素・抗体/TCRのスクリーニングでは、探索規模(ライブラリサイズ)と評価系の再現性が成果を左右します。DMSCSは、マイクロ流体技術を用いてサンプルと試薬を精密に制御し、1ドロップレット=1マイクロリアクターとして単離・反応・評価を行うことで、シングルセル・スクリーニング実験系の構築を支援する研究用装置です。
シングルセル ドロップレットジェネレーター DMSCSシリーズとは
DMSCS(Single Cell Droplet Generator)は、細胞・微生物・ビーズなどの懸濁液と試薬をマイクロ流路内で正確に混合し、マイクロサイズのドロップレット(エマルジョン)へ封入・単離する装置です。ドロップレットを反応場として用いたスクリーニング実験系は、探索数の拡大と評価感度の向上を両立し、研究のボトルネックを解消する有効な選択肢になります。
既存の実験環境と組み合わせやすい設計思想(後工程に既存セルソーター・FACS等を活用)
DMSCSシリーズは、スクリーニングにおけるドロップレット生成・反応工程(封入・混合・反応)を担う装置として設計されています。そのため、後工程では、研究室やコア施設で運用されている既存のセルソーター・FACS、蛍光顕微鏡、PCR装置、培養・解析機器などを活用しやすい構成です。
ドロップレット技術の導入形態には複数の考え方があり、分取・回収までを一体的に扱う構成も選択肢の一つです。一方で、既存設備を活かして工程ごとに最適化する運用は、スクリーニング実験系の設計や条件検討、再現性確保、設備更新の柔軟性という点で適する場合があります。DMSCSは、こうした研究現場での実装を想定し、既存ワークフローに組み込みやすいことを重視しています。
DMSCSの主な研究用途
- ドロップレットPCR・シングルセルRT-PCR
- 酵素スクリーニング実験系(蛍光・比色などの反応指標)
- 微生物スクリーニング実験系/高生産株評価
- 抗体・TCRスクリーニング実験系(結合・反応・分泌指標など)
- FACS・ソーティング、GMD-FACS(前処理・連携)
- ドロップレット培養・共培養
▶ DMSCSが適しているケース
- 既存のセルソーター/FACSや解析機器を活用したい場合
ドロップレット内で反応や指標付与を行い、後工程の選別・解析は既存設備で行うスクリーニング実験系を構築したい場合に適しています。 - 評価指標や反応条件を研究内容に合わせて設計したい場合
蛍光反応、酵素反応、分泌評価、ゲル化条件などを目的に応じて柔軟に検討・最適化したい場合に向いています。 - 探索規模を拡大し、分布として活性を評価したい場合
微生物・酵素・抗体などにおいて、個体差・クローン差を単一反応単位で捉えたいケースに有効です。 - 既存の実験フローを大きく変えずにスクリーニングを高度化したい場合
現行の培養・解析・選別工程を活かしつつ、スクリーニング実験系の自由度を高めたい研究に適しています。
▶ DMSCSが必ずしも最適とは限らないケース
- 評価対象数が少なく、ハイスループット性を必要としない場合
数十〜数百サンプルの評価が主であれば、マイクロプレート等の手法の方が効率的な場合があります。 - 分取・回収までを単一の装置系統で完結させる必要がある場合
実験設計上、一体的な自動選別が前提となる研究では、本装置と異なる仕組みが適する可能性があります。 - ドロップレット内での反応設計や条件検討が困難な評価系
長期間の複雑操作や、ドロップレット内で再現しにくい物理操作が中心となる実験では、適合性の検討が必要です。 - 実験手順や評価プロセスを固定化された形で運用したい場合
本装置は、シングルセル・スクリーニング実験系の設計や条件検討に関与しながら進める研究スタイルを想定しています。あらかじめ定義された手順に沿って実験を完結させたい場合には、別のアプローチが適することがあります。
※適合性は研究目的・設備環境により異なります。研究内容に応じて、装置構成やワークフローを個別にご提案します。
DMSCSをより有効に活用いただくためのQ&A
Q1:DMSCSは、どのような役割の生成装置で、どんな研究スタイルに向いていますか?
A:DMSCSは、シングルセル・スクリーニング実験系におけるドロップレット生成・反応工程(封入・混合・反応・評価指標付与)を構築するための研究用装置です。研究目的に応じて評価指標や反応条件、ワークフローを検討・設計する研究スタイルを想定しており、実験系の設計や条件検討に主体的に関与する研究・開発に適しています。
Q2:分取・回収や選別まで含めて、DMSCSだけで完結しますか?
A:DMSCSは、ドロップレット内での混合・反応工程までを担う装置として設計されています。分取・回収や詳細な分析・解析については、既存のセルソーター(FACS)や解析機器と組み合わせて運用することを前提としています。
Q3:細胞や微生物をシングルセル化する一般的なドロップレットジェネレーターと同等ですか?
A:本製品は、一般的なドロップレットジェネレーターとの同等性比較や代替を目的とした製品ではありません。実験系構築や独自の実験プロセスを前提としない、仕様や価格のみでの比較をご希望の場合には、他社製品の方が適している可能性があります。
多様なサンプル封入・単離と目的別ドロップレット形式
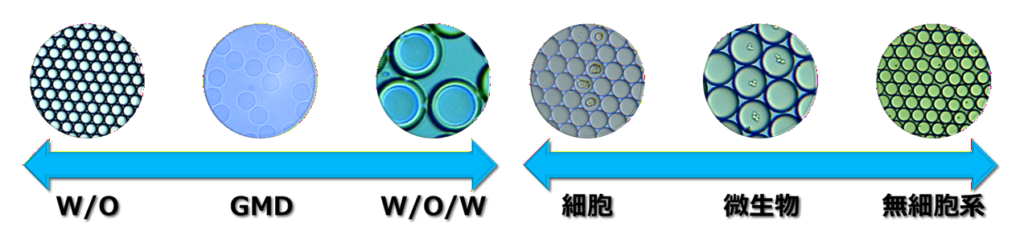
動物細胞、植物細胞、微生物、無細胞系、オリゴ修飾ビーズなど多様なサンプルをハイスループットでドロップレットに封入・単離し、個別のマイクロリアクターとして取り扱えます。
一般的なW/Oシングルエマルジョンに加え、GMD(ゲルマイクロドロップレット)やW/O/Wダブルエマルジョンなど、研究目的に応じたドロップレット(エマルジョン)形式の生成に対応します。
※ダブルエマルジョン(W/O/W)作製機能はオプションです。
DMSCSシリーズの技術的特長
- 高速性:生成速度 ~60万個/分(※)
- 高出力:最高圧 700kPa(※)、高粘度液や微細流路にも対応しやすい
- 高精度:CV≦5%(※)、単分散・高再現性のドロップレット生成
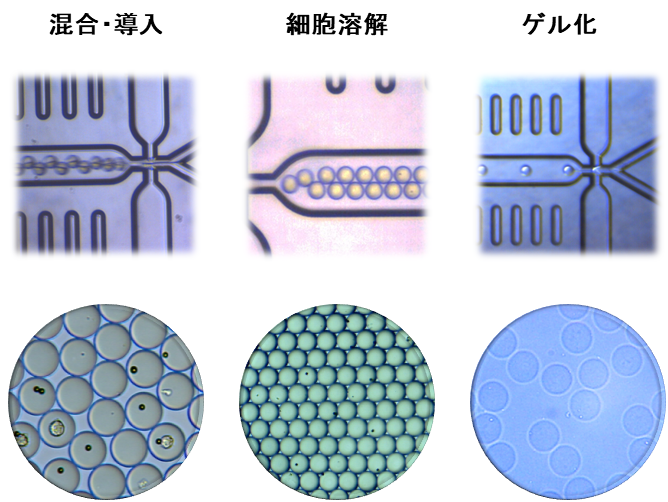
- 液混合:2液混合チップにより、ドロップレット内混合・導入、細胞溶解、ゲル化などを実現
- 多様性:数µm~300µmの範囲で、W/O、O/W、GMD、W/O/W生成に対応(※)
- 温調器:温調機能オプション(0~100℃、※)で保冷~ゲルビーズ作製まで対応
- 拡張性:ユニット・オプションの段階的導入や、研究進捗に応じた複合化が可能
- 支援性:DIY部品販売ではなく、装置組立・据付・講習・プロトコル検討の支援を含む
※装置構成、オプション選択、プロトコル条件により性能は変わります。
ドロップレット内での混合・調製と単離(ワークフローイメージ)
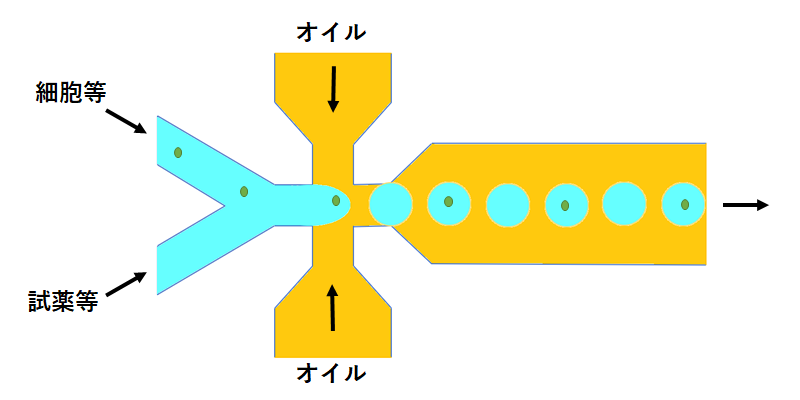
細胞、微生物、ビーズなどのサンプル懸濁液を直径数µm~数百µmのドロップレットにハイスループットで単離し、マイクロ流路合流部で混合・導入される試薬や溶液を用いた細胞溶解、mRNA捕捉、抗原抗体反応、蛍光反応、PCRサイクル、ゲル化等の各種操作を、個別のマイクロリアクターであるドロップレット内で行うことができます。後工程は、既存のFACS/ソーターや解析機器と組み合わせて研究目的に応じた構成を設計できます。
DMSCSの装置構成・価格例
DMSCSは、実験系構築を前提とした研究開発向け装置であり、用途や実験内容に応じて必要な構成が異なります。本ページに掲載している装置構成および価格は、研究目的や工程条件が明確なケースを想定した参考例です。
実際の装置構成や価格は、研究目的や実験内容に応じて構成が調整されるため、あらかじめ定型化された一律価格でのご案内は行っておりません。
※税抜360万円以下の構成については、想定する実験内容や工程条件によって、必要な性能や再現性の実現可否が条件依存となる場合があります。
※2026年4月1日現在
| タイプ | 最高出力圧 | 生成速度 | 送液系統 | 流量センサー | 標準単価(税抜) WEB単価(税抜) |
|---|---|---|---|---|---|
| 最小限特殊構成 | 要ご相談 | 要ご相談 | 要ご相談 | 要ご相談 | ¥2,700,000~ |
| E-2CHタイプ | 200kPa (2000mbar) | ~30万個/分※ | 2液系 | オプション | お問い合わせ |
| E-3CHタイプ | 200kPa (2000mbar) | ~30万個/分※ | 3液系 | オプション | お問い合わせ |
| E-3CH温調タイプ | 200kPa (2000mbar) | ~30万個/分※ | 3液系 | オプション | お問い合わせ |
| H-3CH温調タイプ | 700kPa (7000mbar) | ~60万個/分※ | 3液系 | 3液系 | お問い合わせ |
| その他構成・タイプ | お打ち合わせ | お打ち合わせ | お打ち合わせ | お打ち合わせ | お問い合わせ |
※装置価格は商流や購入時期により異なります。ご検討の際は都度お見積をご依頼ください。
※実際の見積価格は、個別の装置構成、オプション機能、仕様条件により増減します。
※消耗品・試薬類は上記装置参考価格には含まれておりません。
※お届け先や条件により、運送費、搬入・据付・組立設置費、出張費等を別途加算させていただく場合があります。
シングルセルドロップレットジェネレーター DMSCS関連カタログ
シングルセルドロップレットジェネレーター DMSCSシリーズ
マイクロドロップレット生成試薬 008-FluoroSurfactant
※本製品は、試験研究用です。ヒトまたは動物用の臨床診断や医療用機器等の用途に用いることはできません。
参考文献
参考文献一覧(クリックで展開)
- Bernath, Kalia et al. “In vitro compartmentalization by double emulsions: sorting and gene enrichment by fluorescence activated cell sorting.” Analytical biochemistry vol. 325,1 (2004): 151-7. doi:10.1016/j.ab.2003.10.005
- Brower, Kara K et al. “Double emulsion flow cytometry with high-throughput single droplet isolation and nucleic acid recovery.” Lab on a chip vol. 20,12 (2020): 2062-2074. doi:10.1039/d0lc00261e
- Chaipan C et al. “Single-Virus Droplet Microfluidics for High-Throughput Screening of Neutralizing Epitopes on HIV Particles.” Cell Chem Biol. 2017 Jun 22;24(6):751-757.e3. doi: 10.1016/j.chembiol.2017.05.009.
- Gérard, Annabelle et al. “High-throughput single-cell activity-based screening and sequencing of antibodies using droplet microfluidics.” Nature biotechnology vol. 38,6 (2020): 715-721. doi:10.1038/s41587-020-0466-7
- Kim, Samuel C et al. “Single-Cell RT-PCR in Microfluidic Droplets with Integrated Chemical Lysis.” Analytical chemistry vol. 90,2 (2018): 1273-1279. doi:10.1021/acs.analchem.7b04050
- Lance, Shea T et al. “Peering below the diffraction limit: robust and specific sorting of viruses with flow cytometry.” Virology journal vol. 13,1 201. 1 Dec. 2016, doi:10.1186/s12985-016-0655-7
- Fang, Yongliang et al. “Going native: Direct high throughput screening of secreted full-length IgG antibodies against cell membrane proteins.” mAbs vol. 9,8 (2017): 1253-1261. doi:10.1080/19420862.2017.1381812
- Gérard, Annabelle et al. “High-throughput single-cell activity-based screening and sequencing of antibodies using droplet microfluidics.” Nature biotechnology vol. 38,6 (2020): 715-721. doi:10.1038/s41587-020-0466-7
- Lance, Shea T et al. “Peering below the diffraction limit: robust and specific sorting of viruses with flow cytometry.” Virology journal vol. 13,1 201. 1 Dec. 2016, doi:10.1186/s12985-016-0655-7
- Lu, Heng et al. “High throughput single cell counting in droplet-based microfluidics.” Scientific reports vol. 7,1 1366. 2 May. 2017, doi:10.1038/s41598-017-01454-4
- Luo, Siwei et al. “ATLAS-seq: a microfluidic single-cell TCR screen for antigen-reactive TCRs.” Nature communications vol. 16,1 216. 2 Jan. 2025, doi:10.1038/s41467-024-54675-3
- McDaniel JR et al. “Ultra-high-throughput sequencing of the immune receptor repertoire from millions of lymphocytes.” Nat Protoc. 2016 Mar;11(3):429-42. doi:10.1038/nprot.2016.024.
- Potenza, Luca et al. “Passive Droplet Microfluidic Platform for High-Throughput Screening of Microbial Proteolytic Activity.” Analytical chemistry vol. 96,40 (2024): 15931-15940. doi:10.1021/acs.analchem.4c02979
- Rajan, Saravanan et al. “Recombinant human B cell repertoires enable screening for rare, specific, and natively paired antibodies.” Communications biology vol. 1 5. 22 Jan. 2018, doi:10.1038/s42003-017-0006-2
- Reece, Amy et al. “Microfluidic techniques for high throughput single cell analysis.” Current opinion in biotechnology vol. 40 (2016): 90-96. doi:10.1016/j.copbio.2016.02.015
- Rotem, Assaf et al. “Single-cell ChIP-seq reveals cell subpopulations defined by chromatin state.” Nature biotechnology vol. 33,11 (2015): 1165-72. doi:10.1038/nbt.3383
- Saikia, Mridusmita et al. “Simultaneous multiplexed amplicon sequencing and transcriptome profiling in single cells.” Nature methods vol. 16,1 (2019): 59-62. doi:10.1038/s41592-018-0259-9
- Schaerli, Yolanda. “Bacterial Microcolonies in Gel Beads for High-throughput Screening.” Bio-protocol vol. 8,13 (2018): e2911. doi:10.21769/BioProtoc.2911
- Segaliny, AI. et al. “Functional TCR T cell screening using single-cell droplet microfluidics.” Lab Chip, 2018,18, 3733-3749. doi:10.1039/c8lc00818c
- Shembekar, Nachiket et al. “Single-Cell Droplet Microfluidic Screening for Antibodies Specifically Binding to Target Cells.” Cell reports vol. 22,8 (2018): 2206-2215. doi:10.1016/j.celrep.2018.01.071
- Sinha, Nidhi et al. “Integrating Immunology and Microfluidics for Single Immune Cell Analysis.” Frontiers in immunology vol. 9 2373. 16 Oct. 2018, doi:10.3389/fimmu.2018.02373
- Spindler, Matthew J et al. “Massively parallel interrogation and mining of natively paired human TCRαβ repertoires.” Nature biotechnology vol. 38,5 (2020): 609-619. doi:10.1038/s41587-020-0438-y
- Staskiewicz, Klaudia et al. “Droplet microfluidic system for high throughput and passive selection of bacteria producing biosurfactants.” Lab on a chip vol. 24,7 1947-1956. 26 Mar. 2024, doi:10.1039/d3lc00656e
- Sukovich, David J et al. “Bulk double emulsification for flow cytometric analysis of microfluidic droplets.” The Analyst vol. 142,24 (2017): 4618-4622. doi:10.1039/c7an01695f
- Wen, Na et al. “Development of Droplet Microfluidics Enabling High-Throughput Single-Cell Analysis.” Molecules (Basel, Switzerland) vol. 21,7 881. 5 Jul. 2016, doi:10.3390/molecules21070881
- Wimmers, F. et al. “Single-cell analysis reveals that stochasticity and paracrine signaling control interferon-alpha production by plasmacytoid dendritic cells.” Nat Commun 9, 3317 (2018). doi:10.1038/s41467-018-05784-3
- Zhang, Qiang et al. “Development of a facile droplet-based single-cell isolation platform for cultivation and genomic analysis in microorganisms.” Scientific reports vol. 7 41192. 23 Jan. 2017, doi:10.1038/srep41192
- Zhang, Ying et al. “A programmable microenvironment for cellular studies via microfluidics-generated double emulsions.” Biomaterials vol. 34,19 (2013): 4564-72. doi:10.1016/j.biomaterials.2013.03.002
- Zheng, Wenshan et al. “High-throughput, single-microbe genomics with strain resolution, applied to a human gut microbiome.” Science (New York, N.Y.) vol. 376,6597 (2022): eabm1483. doi:10.1126/science.abm1483
- Zhu, Zhi, and Chaoyong James Yang. “Hydrogel Droplet Microfluidics for High-Throughput Single Molecule/Cell Analysis.” Accounts of chemical research vol. 50,1 (2017): 22-31. doi:10.1021/acs.accounts.6b00370
- Zinchenko, Anastasia et al. “One in a million: flow cytometric sorting of single cell-lysate assays in monodisperse picolitre double emulsion droplets for directed evolution.” Analytical chemistry vol. 86,5 (2014): 2526-33. doi:10.1021/ac403585p
